|
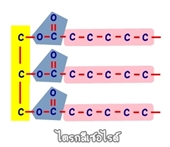
ถ้าอธิบายโดยอ้างอิงจากรูปนี้ ในไขมันหรือน้ำมัน 1 โมเลกุล ประกอบด้วยแกนกลาง , หัว และหางที่เป็นเส้นยาวๆ
แกนกลาง (สีเหลือง) : เป็นอะตอมของ C (คาร์บอน) และ H (ไฮโดรเจน) ล้วนๆ (ส่วนนี้ภายหลังจะกลายร่าง
เป็นกลีเซอรีน)
หัว (สีฟ้า) : เป็นส่วนที่แสดงเอกลักษณ์ เรียกเป็นภาษาทางเคมีว่าหมู่ฟังก์ชันซึ่งเป็นส่วนสำคัญที่ทำให้เกิดกลไก
หรือปฏิกิริยาต่างๆ
หางยาวๆ (สีชมพู) : ประกอบด้วย C และ H ต่อกันเยอะๆ เป็นสายโซ่ยาว ในธรรมชาติมักพบ C หรือคาร์บอน
16-18 ตัวต่อกัน
อาจด้วยพันธะเดี่ยวทั้งหมด หรือมีพันธะคู่ด้วยก็ได้
พันธะเดี่ยว คือคาร์บอนทั้ง 16-18 ตัวนั้น มันจะจับกันแบบนี้ -C-C-C-C- เป็นที่มาของคำว่า "อิ่มตัว" คือไม่มีแขนว่าง
พอจะไปจับกะใครเขาได้อีก
แต่ถ้าพันธะคู่ คือบางตำแหน่งจะจับกันแบบนี้ -C-C=C-C- และก็เลยเป็นที่มาของคำว่า "ไม่อิ่มตัว" คือยังมีแขนว่าง
ซ่อนอยู่ สามารถจะเอื้อมไปดึงบุคคลที่สามเข้ามาในชีวิตได้เสมอถ้าโอกาสเหมาะสมนะ
เฉพาะส่วนหัวสีฟ้ารวมทั้งหางด้วยนี้ เราเรียกมันว่ากรดไขมัน(Fatty acid) ซึ่งเป็นส่วนที่ทำให้น้ำมันแต่ละชนิด
แตกต่างกันค่ะ ใน 1 โมเลกุล หาง 3 เส้นนี้อาจเหมือนหรือต่างกันก็ได้นะคะ เช่นแบบนี้
เช่นแบบนี้ 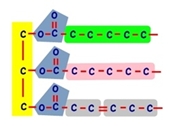 |
|
| |
หรือจะเป็นแบบนี้ 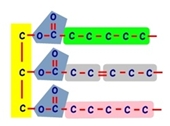 |
สังเกตดูจะเห็นว่าทั้งสองรูปบน มี fatty acid สามเส้น คือเขียว ชมพู และเทา แต่อยู่ในลำดับที่แตกต่างกัน ทำให้
คุณสมบัติของไตรกลีเซอไรด์ทั้งสองโมเลกุลนี้จะต่างกันทันที แม้มันจะประกอบด้วยหางสีเขียว เทา และชมพู
ที่เหมือนๆ กันก็ตาม
ชนิดและลำดับของ fatty acid นี่ล่ะที่ส่งผลต่อคุณสมบัติของสบู่ว่าจะให้ฟองมาก-น้อย , สบู่ก้อนแข็ง-อ่อน เป็นต้น
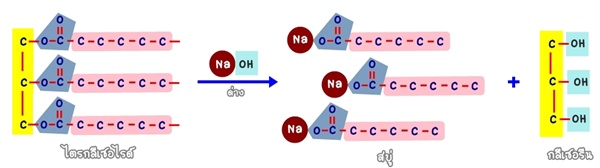
ลองดูซิว่า พอไขมันหรือน้ำมันมาเจอกับด่าง (ในที่นี้คือโซเดียมไฮดรอกไซด์) จะเกิดอะไรขึ้น
นั่นไงคะ! เห็นโมเลกุลที่รูปร่างเหมือนดักแด้รึเปล่า นั่นแหละสบู่ของเราล่ะ
ด่างจะวิ่งเข้าไปจับคู่กับหางทั้ง 3 ของไขมัน ด่าง 1 โมเลกุลก็จับคู่กับหางยาวๆ 1 เส้น ดังนั้นต้องใช้ด่าง 3 โมเลกุล
จึงจะครบคู่พอดี พร้อมกับได้สารอีกตัวหนึ่งแถมมาเป็นผลผลิตด้วย มันก็คือกลีเซอรีนนั่นเองค่ะ
ในสบู่ CP กลีเซอรีนจะยังอยู่ในเนื้อสบู่เต็มที่ แต่ในการผลิตเชิงอุตสาหกรรมมันจะถูกสกัดออกไปเพื่อนำไปใช้
ในอุตสาหกรรมต่อเนื่องอื่นๆ
ในทางเคมีโมเลกุลสบู่นี้ เขาจะเรียกเป็น "เกลือ" หรือ "salt" ชนิดหนึ่งนะคะ
พูดถึง salt ก็แสดงว่าเกี่ยวข้องกับการแตกตัวให้ประจุบวก ประจุลบ แสดงถึงความมีขั้ว(Polar) อะไรที่ขั้วเหมือนกัน
ก็จะเข้าพวกกันได้ ถ้าต่างกันก็อยู่ด้วยกันไม่ได้นะ
เช่น น้ำ+น้ำมัน โดยทั่วไปจะเห็นมันแยกชั้นเพราะน้ำมันไม่มีขั้ว
แต่น้ำมีขั้ว ก็ต่างคนต่างอยู่ไป (แต่ใช่ว่าจะไม่ละลายกันเสียทีเดียว
ขึ้นอยู่กับ degree ความมีขั้วของสารแต่ละประเภท
ด้วย เช่น น้ำมันเบนซีนละลายน้ำได้บางส่วน)
แต่โมเลกุลของสบู่เนี่ยไม่ธรรมดานะพี่น้อง เพราะมันมีทั้งส่วนที่มีขั้วและไม่มีขั้วอยู่ในโมเลกุลเดียวกัน เรียกว่า
2 in 1 น่ะ
แล้วแกจะเอายังไงกับชีวิตล่ะเนี่ย...
มันก็เลยจำต้องแสดงพฤติกรรมแบบรักพี่เสียดายน้องค่ะ คือเมื่อเราใช้สบู่อาบน้ำ โมเลกุลสบู่จะหันส่วนหัวกลมซึ่งมีขั้ว
เข้าหาน้ำ ส่วนหางยาวๆ นั่นก็จะจับกับสิ่งสกปรกเช่นพวกน้ำมันที่อยู่บนผิวหนังเราซึ่งไม่มีขั้ว มองคล้ายๆ กับว่า
มันทำหน้าที่เหมือนสะพานเชื่อมระหว่างน้ำกับสิ่งสกปรก(หรือน้ำมันบนตัวเรา) นั่นเอง
แต่ถ้าบ้านเราเป็นน้ำบาดาลหรือเป็นน้ำกระด้าง โมเลกุลสบู่จะเดี้ยงสนิท แคลเซียม , แมกนีเซียม ซึ่งมีอยู่ปริมาณมาก
ในน้ำกระด้าง จะไปขัดขวางการทำงานของมันโดยเข้าไปจับคู่กับส่วนหางยาวๆ เกิดเป็นสารที่ละลายได้ยากมากๆ
ก็เลยมองเห็นเป็นตะกอนที่เราเรียกกันว่าไคลสบู่นั่นแหละค่ะ
หลังจากนี้ หากเราทำสบู่ซัก Batch นึง ลองจินตภาพตามไปด้วยก็ได้นะคะว่า มีเกิดอะไรขึ้นในหม้อกวนสบู่ของเรา
หวังว่าวันนี้คงจะได้ความรู้กันพอหอมปากหอมคอนะคะ
เจอกันใหม่เมื่อชาติต้องการจ้า  |